1
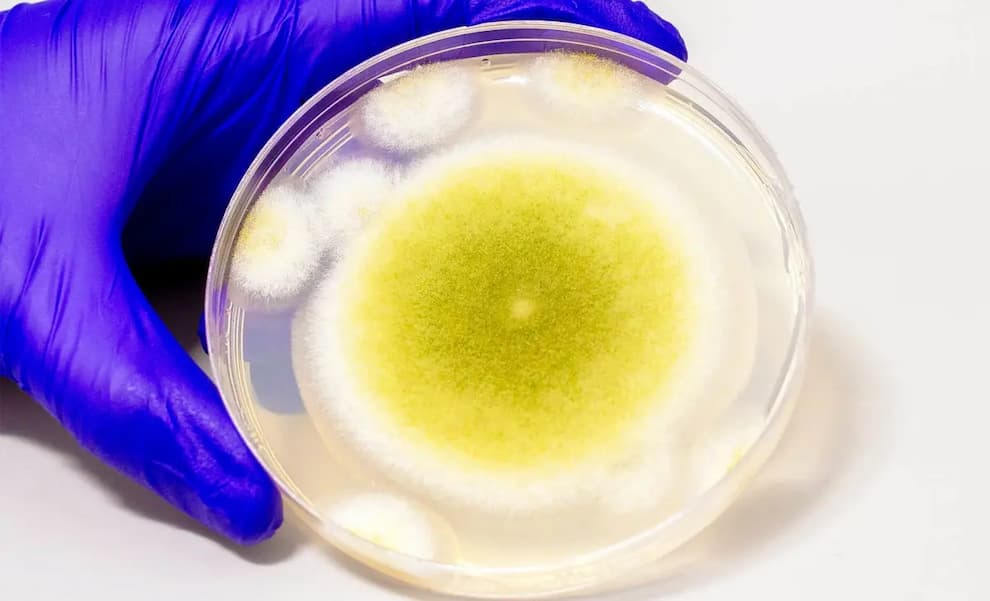
در دهه ۱۹۲۰، کپک زردرنگ Aspergillus flavus شهرتی مرگبار پیدا کرد؛ اعضای تیم هاوارد کارتر پس از باز کردن مقبره توتعنخآمون جان خود را از دست دادند.
چندین دهه بعد، سرنوشت مشابهی برای دانشمندانی که وارد آرامگاه شاه کازیمیر چهارم در لهستان شدند رقم خورد. در عرض چند هفته، ۱۰ نفر از ۱۲ محقق به بیماری تنفسی مبتلا شدند و بررسیها منبع این بیماری مرگبار را به هاگهای خفته A. flavus نسبت دادند.
کشف جدید: از کپک سمی تا داروی ضد سرطان
مدتها بود که Aspergillus flavus تنها به عنوان کپکی سمی شناخته میشد، اما اکنون این کپک نقشی جدید یافته است: تولید ترکیباتی که عملکردی مشابه داروهای معتبر درمان سرطان خون میلوئید حاد (AML) دارند.
آشنایی با Aspergillus flavus
این قارچ بهطور طبیعی در خاک، گیاهان در حال پوسیدگی و غلات یافت میشود. محیطهای گرم و مرطوب بهترین شرایط برای رشد آن هستند و به همین دلیل، یکی از مشکلات رایج در کشاورزی به ویژه در محصولات ذرت، بادام زمینی و مغزها محسوب میشود.
نگرانی اصلی: تولید آفلاتوکسین
موضوع نگرانکننده در مورد این قارچ، توانایی تولید آفلاتوکسینها است؛ ترکیباتی بسیار سمی و سرطانزا که وجود آنها در غذا میتواند خطرات جدی برای سلامت انسان و دام ایجاد کند. به همین دلیل، صنایع غذایی موظف به اجرای مقررات سختگیرانه و انجام آزمایشهای منظم هستند.
نقشه گنج مولکولی کپک
تحول مهم این پژوهش در آزمایشگاه شری گائو در دانشگاه پنسیلوانیا رخ داد؛ جایی که محققان به دنبال کشف داروهای پنهان در ژنوم میکروبها هستند.
تمرکز بر RiPP ها
این تیم تحقیقاتی بر روی پپتیدهای حلقوی کوچک موسوم به RiPP (پپتیدهای سنتز شده ریبوزومی و اصلاح شده پس از ترجمه) تمرکز کرد؛ مولکولهایی که به دلیل فعالیت زیستی پیچیده خود شناخته میشوند. تاکنون هزاران RiPP در باکتریها شناسایی شده اما فقط تعداد محدودی در قارچها یافت شده است.
چالشهای شناسایی RiPP ها
کیویو نیه، نویسنده اصلی مقاله و پژوهشگر فوقدکتری در دانشگاه پنسیلوانیا توضیح داد: «خالصسازی این مواد بسیار دشوار است.» علاوه بر این، شناسایی ژنهایی که سنتز این ترکیبات را هدایت میکنند، بهراحتی قابل چشمپوشی است.
استراتژی دوگانه برای کشف
محققان ابتدا اثر انگشت شیمیایی دوازده گونه مختلف از Aspergillus را مقایسه کردند و سپس روی خوشههای ژنی که احتمال میدادند مسئول تولید RiPP باشند، متمرکز شدند.
با خاموش کردن این ژنها، قلههای شیمیایی مشکوک ناپدید شد و این موضوع تأیید کرد که آنها کارخانه فعال RiPP را در دل کپک مقبره پیدا کردهاند.
از کپک مقبره تا داروی ضد سرطان
تجزیه و تحلیل ساختاری منجر به کشف چهار مولکول کاملاً جدید با ساختار پیچیده حلقههای بههمپیوسته شد. محققان این ترکیبات را «آسپیریجیمایسین» نامیدند؛ برگرفته از نام قارچ سازنده آن.
اثر ضدسرطانی آسپیریجیمایسینها
دو مورد از این چهار مولکول به طور مستقیم فعالیت قابل توجهی علیه سلولهای سرطان خون نشان دادند اما یک تغییر شیمیایی ساده توانست این اثر را به طور چشمگیر افزایش دهد.
با افزودن یک زنجیره چربی مشابه همان که در ژل رویال (مادهای مغذی که لاروهای معمولی زنبور را به ملکه تبدیل میکند) یافت میشود، محققان نسخهای اصلاحشده از آسپیریجیمایسین تولید کردند که عملکرد آن با داروهای قدیمی سرطان خون مانند سیتارابین و دانوروبیسین برابری میکند.
مکانیسم ورود دارو به سلول
چرا افزودن این زنجیره چربی قدرت دارو را چند برابر کرد؟ گروه گائو با استفاده از صفحهنمایش مبتنی بر CRISPR ژنهای مختلف سلولهای سرطان خون را حذف کردند و تغییرات در جذب دارو را رصد کردند.
نقش کلیدی SLC46A3
نتایج نشان داد که یک ناقل به نام SLC46A3 برای ورود دارو حیاتی است. این پروتئین معمولاً مواد مغذی را از لیزوزومها (بخش بازیافت سلول) منتقل میکند. پژوهشگران متوجه شدند که زنجیره چربی، آسپیریجیمایسینهای مشتقشده از کپک را قادر میسازد از این مسیر وارد سلول شوند.
نیه توضیح داد: «این ژن مانند دروازه عمل میکند. دانستن اینکه لیپیدها میتوانند بر نحوه انتقال این ژن تأثیر بگذارند، ابزاری جدید برای توسعه داروها در اختیار ما میگذارد.»
این یافته میتواند به نجات سایر پپتیدهای حلقوی که به دلیل ضعف در عبور از موانع سلولی در آزمایشهای بالینی شکست میخورند، کمک کند.
مقابله با تقسیم سلولی سرطان
بررسیهای میکروسکوپی و آزمایشهای بیوشیمیایی نشان داد که آسپیریجیمایسینهای اصلاحشده با مختل کردن میکروتوبولها (سازههای پروتئینی که مسئول جدا کردن کروموزومها در طول میتوز هستند) رشد تومور را متوقف میکنند.
ویژگی منحصر بهفرد: اثر انتخابی
جالب است که این مولکولهای مشتقشده از کپک تأثیر چندانی بر روی سلولهای سرطانی پستان، کبد و ریه و همچنین بر طیف وسیعی از باکتریها و مخمرها نداشتند.
این انتخابگری نشان میدهد که دارو میتواند با عوارض جانبی کمتری نسبت به داروهای شیمیدرمانی سنتی همراه باشد که معمولاً تمام سلولهای در حال تقسیم سریع را هدف قرار میدهند.
پاسخهای مدرن از کپکهای باستانی
برای دههها، دانشمندان درباره نحوه ساخت RiPP ها در قارچها دچار سردرگمی بودند و گاهی آنها را با پپتیدهای غیر ریبوزومی اشتباه میگرفتند. این مطالعه توانست این معما را حل کند و امضای شیمیایی این ترکیبات را به ژنهای مسئول پیوند دهد.
نیه گفت: «سنتز این ترکیبات بسیار پیچیده است اما همین پیچیدگی باعث فعالیت زیستی چشمگیر آنها میشود.»
آینده اکتشافات دارویی
اسکنهای ژنومی مقایسهای تاکنون وجود خوشههای ژنی مشابه RiPP را در دهها کپک دیگر نشان داده است که احتمال کشف مولکولهایی با خواص آنتیبیوتیکی، ضدویروسی یا تعدیلکننده سیستم ایمنی را افزایش میدهد. به گفته نیه، این حوزهای کشفنشده با پتانسیل فوقالعاده است.
مسیر از مقبره تا آزمایش بالینی
گام بعدی، آزمایش آسپیریجیمایسینها بر روی موشها برای ارزیابی سمیت، دوز مناسب و اثربخشی در موجودات زنده است. در صورت موفقیت، مسیر برای آزمایشهای انسانی هموار خواهد شد.
گائو با تأمل بر این مسیر که از افسانههای مقبره تا آزمایشگاه طی شده است، به یک اصل مهم اشاره میکند: «قارچها به ما پنیسیلین دادند. این نتایج نشان میدهد که هنوز داروهای زیادی از منابع طبیعی باقی مانده که باید کشف شوند.»
سخن پایانی
طبیعت هنوز گنجینههای درمانی کشفنشدهای در خود دارد. با پیشرفتهای مستمر در استخراج ژنومی و مهندسی ترکیبات، مرز بین خطرات میکروبی و معجزات پزشکی روزبهروز باریکتر میشود.
این موفقیتها گواهی بر نبوغ شیمیایی طبیعت و جسارت دانشمندانی است که در کپکها و میکروبها به دنبال داروهای نجاتبخش آینده هستند.
این مطالعه در مجله Nature Chemical Biology منتشر شده است.
source